- Het genezingspotentieel van nanotechnologie
- Het oog met duizenden nanobots doordringen
- Innovatieve manieren om kanker te bestrijden
- Kunnen we beschadigde organen straks met één enkele aanraking ‘repareren’?
- Nanobots – de sleutel tot een langer leven?
De moderne geneeskunde heeft de afgelopen 100 jaar enorme ontwikkelingen doorgemaakt, waardoor de menselijke levensduur aanzienlijk is verlengd. Sommige ziektes die vroeger aan miljoenen mensen het leven kostten zijn volledig uitgeroeid. Voor andere zijn er nieuwere, effectievere behandelingen ontwikkeld. Het sterftecijfer onder mensen die lijden aan medische aandoeningen als kanker blijft helaas nog steeds hoog.
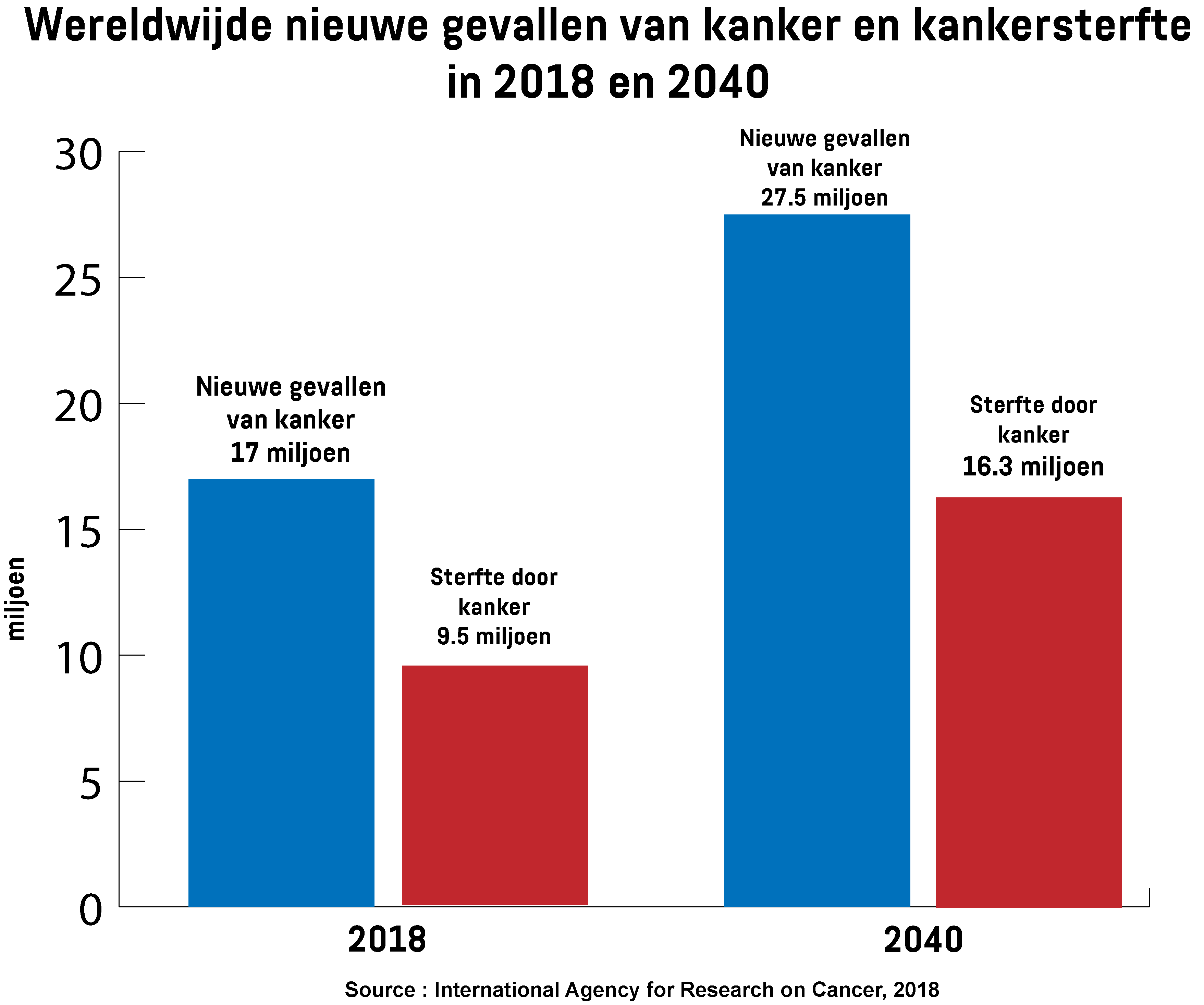
Volgens het International Agency for Research on Cancer (IARC) werden er in 2018 wereldwijd naar schatting 17 miljoen nieuwe gevallen van kanker gediagnosticeerd en overleden er 9,5 miljoen mensen aan de gevolgen van deze ziekte. Naarmate de wereldbevolking blijft groeien en ouder wordt, zullen deze cijfers tegen 2040 naar verwachting nog verder gestegen zijn, tot 27,5 miljoen nieuwe gevallen van kanker en 16,3 miljoen kanker-gerelateerde sterfgevallen.

Bovendien is zelfs de moderne geneeskunde vaak volledig hulpeloos als het gaat om het helen van zwaar beschadigde organen. Nanotech is mogelijk een oplossing voor deze uitdagingen. Met deze revolutionaire technologie zijn nieuwe manieren mogelijk om ziekten te genezen en menselijke cellen te herstellen. Sterker nog, de verwachtingen zijn dat de wereldwijde nanomedische markt tegen 2022 een waarde van $293,1 miljard zal bereiken.
Het genezingspotentieel van nanotechnologie
Nanotechnologie kan worden gedefinieerd als de manipulatie van individuele atomen en moleculen om machientjes op nanoschaal te kunnen ontwikkelen (een nanometer is één miljardste van een meter). Nanotechnologie kent een breed scala aan potentiële toepassingen in uiteenlopende gebieden, waaronder scheikunde, biologie, natuurkunde, engineering, materiaalwetenschap en vele andere. In dit artikel gaan we het hebben over medische toepassingen, waarbij nanotechnologie een steeds belangrijker, levensverlengend instrument wordt.
Er zijn twee belangrijke gebieden waarin nanotechnologie kan worden toegepast. Ten eerste kan het mogelijk korte metten maken met levensbedreigende ziekten als kanker of hartaandoeningen. Ten tweede kan het ingezet worden voor het herstellen van schade die door ons lichaam op cellulair niveau wordt veroorzaakt. Maar andere potentiële toepassingen van nanotechnologie omvatten ziektediagnostiek, gerichte medicijnafgifte, moleculaire beeldvorming en nog veel meer.
Het oog met duizenden nanobots doordringen
Een internationaal team van wetenschappers, geleid door onderzoekers van het Max Planck Institute for Intelligent Systems in Stuttgart, heeft propellervormige nanobots ontwikkeld die dicht weefsel kunnen penetreren, zoals dat in het glasvocht van het menselijk oog. De nanobots zijn maar 500 nanometer breed – 200 keer kleiner dan de diameter van een mensenhaar en zelfs kleiner dan de breedte van een bacterie. Ze zijn ook bedekt met een antikleefcoating om ze door het oog te laten bewegen zonder schade toe te brengen aan het gevoelige omringende weefsel.
“Voor de coating laten we ons door de natuur inspireren”, vertelt Zhiguang Wu, de eerste auteur van het onderzoek. “Tijdens de tweede stap brachten we een vloeistoflaag aan op de vleesetende werperplant, die een glad oppervlak heeft om insecten te vangen – een soort tefloncoating. Deze gladde laag zorgt ervoor dat het plakkerige biologische eiwitnetwerk in het glasvocht zich niet aan onze nanorobots hecht. Zonder deze gladde laag kunnen onze robotjes zich niet in het oog voortstuwen”. De wetenschappers voegden ook kleine deeltjes magnetische materialen als ijzer toe, zodat de nanobots met behulp van magnetische velden naar de gewenste bestemming gemanoeuvreerd kunnen worden.
De nanobots zijn al met succes getest in het oogziekenhuis van de Universiteit van Tübingen, een van de partners in het project. Tijdens het onderzoek injecteerden de wetenschappers tienduizenden nanobots in het glasvocht van een ontleed varkensoog en gebruikten vervolgens een magnetisch veld om de bots naar het netvlies te leiden. Daarbij werd ook gebruikgemaakt van optische coherentietomografie om de bewegingen te observeren. De hoop is dat we hiermee op een dag nanobots kunnen ontwikkelen die niet alleen door het oog, maar ook door andere soorten weefsels in het menselijk lichaam kunnen bewegen. Deze ontwikkeling is ook een belangrijke stap in de richting van het gebruik van nanobots voor het efficiënt en doelgericht toedienen van medicijnen in hele specifieke delen van het lichaam. “Dat is ons doel”, zegt Tian Qiu, een van de auteurs van het onderzoek. “We willen onze nanopropellers kunnen gebruiken als hulpmiddelen bij de minimaal invasieve behandeling van allerlei soorten ziekten, waarbij het problematische gebied moeilijk te bereiken is en omringd door dicht weefsel. In de nabije toekomst zullen we de nanobots als het ware met medicijnen kunnen opladen”.
Innovatieve manieren om kanker te bestrijden
Wetenschappers van de Arizona State University (ASU) hebben onlangs hun krachten gebundeld met onderzoekers van het National Center for Nanoscience and Technology (NCNST) van de Chinese Academy of Sciences om nanobots te ontwikkelen die tumoren kunnen doen krimpen door de bloedtoevoer ervan af te sluiten. “We hebben het eerste volledig autonome DNA-robotsysteem ontwikkeld voor een zeer precies medicijnontwerp en gerichte kankertherapie”, zegt Hao Yan, directeur van het Center for Molecular Design and Biomimetics van het ASU Biodesign Institute. En omdat alle bloedvaten die de tumorgroei voeden in principe hetzelfde zijn, zijn de wetenschappers van mening dat deze technologie op verschillende soorten kanker toegepast kan worden, waaronder borstkanker, longkanker, eierstokkanker en melanoom.
De wetenschappers hebben succesvolle proeven gedaan met muiskankermodellen. Daarbij werden menselijke kankercellen in muizen geïnjecteerd om agressieve tumorgroei te induceren. Vervolgens werden de nanobots ingebracht om de tumoren te zoeken en te vernietigen. “We kunnen deze nanorobots programmeren om moleculaire ladingen te transporteren waarmee ze ter plaatse de bloedtoevoer naar de tumor verstoren. Dit kan leiden tot weefselsterfte en krimpen van de tumor”, vertelt NCNST-professor Baoquan Ding. De nanobots bestaan uit een plat, rechthoekig opgevouwen DNA-laagje van 90 bij 60 nanometer. Aan het oppervlak wordt het bloedstollende enzym trombine bevestigd dat het bloed in de bloedvaten naar de tumor stolt, waardoor de tumor uiteindelijk sterft. De nanobots zijn geprogrammeerd om door de bloedbaan te reizen en alleen kankercellen aan te vallen zodat gezonde cellen onbeschadigd blijven. Om dit te bereiken, bevestigden de wetenschappers ook een DNA-aptameer aan het oppervlak van de nanobot, die zich specifiek richt op het nucleoline-eiwit op het oppervlak van tumor-endotheelcellen.
Volgens de wetenschappers bleken de nanobots veilig en immunologisch inert te zijn in de weefsels van muizen en grote dieren. Daarbij werden geen veranderingen waargenomen in de normale bloedcoagulatie of celmorfologie. Ze vonden ook geen bewijs dat de nanobots zich in de hersenen verspreid zouden hebben, waar ze mogelijk een beroerte of andere onbedoelde bijwerkingen kunnen veroorzaken. De nanobots waren in staat om de bloedtoevoer naar de tumor binnen 24 uur te blokkeren en weefselbeschadiging te veroorzaken. Daarna werden ze uit het lichaam verwijderd of vernietigd. De wetenschappers observeerden in 3 van de 8 muizen volledige regressie van de tumoren. De mediane overlevingsduur steeg daarbij van 20,5 naar 45 dagen. “De DNA-nanorobot-trombineafgifte is een belangrijke stap in de toepassing van DNA-nanotechnologie voor kankertherapie”, aldus Yan. “Combinaties van verschillende rationeel ontworpen nanorobots met verschillende middelen kunnen helpen om het uiteindelijke doel van kankeronderzoek te bereiken: de uitroeiing van solide tumoren en gevasculariseerde metastasen”.
Met een enigszins andere aanpak hebben onderzoekers van Durham University in het Verenigd Koninkrijk nanobots ontwikkeld die kankercellen binnen 60 seconden kunnen vernietigen. De nanobots zijn uitgerust met lichtgeactiveerde motoren en peptiden waarmee ze kankercellen kunnen identificeren. Bij blootstelling aan ultraviolet licht gaan de motoren met twee tot drie miljoen omwentelingen per seconde draaien. Hiermee breken ze door de membranen van de kankercellen waardoor deze vernietigd worden. Het onderzoek bevindt zich nog in een zeer vroeg stadium en de nanobots zijn tot nu toe alleen getest op micro-organismen en kleine vissen. De onderzoekers hopen echter dat ze binnenkort klinische proeven bij mensen kunnen starten. “We willen deze met licht geactiveerde nanomachines zo snel mogelijk gaan inzetten op borsttumoren en huidmelanomen, ook die resistent zijn tegen bestaande chemotherapie”, zegt dr. Robert Pal van Durham University. “Zodra deze methode volledig ontwikkeld is, kunnen we hiermee een potentiële stapsgewijze verandering in niet-invasieve kankerbehandeling bieden. Hiermee zullen de overlevingspercentages en het welzijn van patiënten wereldwijd aanzienlijk verbeteren”.
Kunnen we beschadigde organen straks met één enkele aanraking ‘repareren’?

Naarmate we ouder worden raakt het DNA in onze cellen beschadigd, wat tot allerlei gezondheidsproblemen kan leiden. Tot nu toe was er geen manier om dit proces om te keren. Maar onderzoekers van het Wexner Medical Center van de Ohio State University en Ohio College of Engineering hebben nu een apparaat ontwikkeld dat zieke organen kan genezen – door de functie van een cel met één enkele aanraking te veranderen. Deze technologie, bekend als Tissue Nanotransfection (TNT), werkt door nieuwe genetische code in levende huidcellen te injecteren en deze om te zetten in een andere soort cel die nodig is voor de behandeling. Hiermee kan beschadigd of verouderd weefsel of de functie ervan hersteld worden. Deze methode kan op verschillende soorten weefsels – zoals organen, bloedvaten en zenuwcellen – toegepast worden. De onderzoekers hebben de methode op muizen met zwaar gewonde poten toegepast en slaagden erin om de ledematen binnen drie weken te genezen door de huidcellen in vasculaire cellen te veranderen. Bovendien wisten ze met deze methode hersenletsel als gevolg van beroertes in muizen te herstellen door ze te injecteren met huidcellen die geherprogrammeerd waren in zenuwcellen.
De behandeling is volgens de onderzoekers 98 procent effectief, duurt minder dan een seconde en is bovendien volledig non-invasief. Het enige dat nodig is om de herprogrammering van de cellen te starten, is een kleine, haast niet merkbare elektrische lading. Bovendien is er geen immunosuppressie nodig omdat de technologie de cellen in het lichaam onder immuunsurveillance houdt. “Met gebruik van onze nieuwe nanochip-technologie kunnen beschadigde of aangetaste organen worden vervangen. We hebben aangetoond dat de huid een vruchtbare broedgrond is waar we de elementen van elk mogelijk aftakelend orgaan kunnen kweken”, zegt Dr. Chandan Sen, de directeur van het Center for Regenerative Medicine en Cell Based Therapies van Ohio State.
Nanobots – de sleutel tot een langer leven?
Nanotechnologie is de laatste jaren een steeds belangrijker instrument geworden in de strijd om onze levensduur te verlengen. In de geneeskunde kan nanotechnologie worden ingezet om dodelijke ziekten als kanker te bestrijden en zelfs om menselijke cellen te repareren of te transformeren. Hoewel veel van het onderzoek op dit gebied zich nog in een zeer vroeg stadium bevindt en het nog jaren kan duren voordat praktische toepassingen mogelijk zijn, menen wetenschappers dat nanotechnologie het antwoord is op veel van onze huidige medische problemen. Het mag nu allemaal nog als sciencefiction klinken, maar het zal waarschijnlijk niet lang meer duren voordat nanobots in ons lichaam virussen, tumoren en andere medische problemen te lijf gaan. Ze bewegen zich vrij door de bloedbaan en verschillende soorten weefsel, op zoek naar tekenen van ziekte of verval en vervolgens gaan ze aan het werk. In de toekomst repareren ze niet alleen individuele cellen, maar ook weefsels en zelfs volledige organen.
Share via:


